更新日期:2025/07/29
更新日期:2025/07/29|
檢驗項目 |
HIV病毒定量檢驗(HIV viral load) |
|
檢驗表單 |
精準醫學暨分子醫學特殊檢驗單(CM-T2A0) |
|
生物參考區間 |
Target Not Detected |
|
危險值及通報值 |
NA |
|
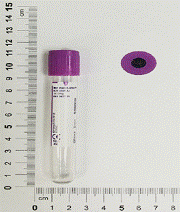
1.採檢容器(圖片)
|
|
|
大紫頭管10mL:標準採檢量 血液 10mL |
|
|
採檢注意事項 (病人準備) |
1.不需空腹 2.檢體採集後將採血管上下顛倒3∼5次。 |
|
檢體傳送要求 |
採檢後全血須於2-25℃盡速傳送,最慢須於24小時內送至 精準診斷組,若無法於24小時內送至 精準診斷組,須先將檢體離心1,600xg,20分鐘後, 血漿分裝至無菌試管中於2-8℃或冷凍於-20℃運送。 |
|
檢體拒收準則 |
檢體量不足或血液凝固 |
|
可送檢時間 |
門診檢驗組:星期一∼星期五 AM 07:00∼PM 22:00 星期六 AM 07:00∼PM 12:00 急診檢驗組:星期一∼星期五24小時收件 星期六 AM 07:00∼PM 12:00 |
|
報告完成時間 |
4個工作天 |
|
加補驗原則/條件 |
不接受加補驗 |
|
檢驗組別及聯絡方式 |
精準診斷組 電話:04-22052121 分機:11202-304 |
|
檢驗方法 |
COBAS6800 (real-time PCR) |
|
檢驗效能 |
請參閱量測不確定度 |
|
檢驗結果的解讀 |
目前市面上有多種針對病毒蛋白酶(protease)、核酸銜接酵素(integrase)、套膜(envelope)和反轉錄酶(reverse transcriptase)之抗反轉錄病毒藥物。不同支系的病毒基因型分析發現了反轉錄酶(reverse transcriptase)、核酸銜接酵素(integrase)和HIV-1 pol之蛋白酶(protease)區內自然發生或藥物誘發的核苷酸(nucleotide)改變、多型性和次要突變,抗藥性試驗變成為HIV-1感染管理重要的診斷工具,患者經序列分析發現可察覺之病毒量增加,便進行抗藥性試驗。病毒量監控可降低抗藥性的風險,臨床上視為病毒大量複製、預告療程中患者病毒演化的警訊指標,多數國家和國際治療準則因此建議應檢測HIV-1病毒量。 多年來治療準則強調,治療的關鍵在於抑制HIV-1病毒量至最低檢測量以下(如50 copies/mL),美國治療準則於2011年開始表示,因部份患者可能有低程度之病毒血症(viremia)而未演變為病毒量突破的現象,ART治療患者之病毒量檢測結果提升至200 copies/mL並不代表治療失敗歐洲的治療準則持續表明病毒量檢測結果應抑制在50 copies/mL以下,病毒最低檢測量的差異對監控治療反應時病毒量檢測結果的臨床解釋,將導致相當不同的結果,而治療的目標是將病毒量抑制在可能出現抗藥性的最低標準以下,該最低標準則尚未明確定義。WHO於2013年7月也開始建議將使用病毒量檢驗的最低資源設定定義為1000 copies/mL做為抑制失敗,需要治療管理決策的門檻。*譯註:response guided therapy,反應引導治療計畫即依病人對藥物的反應量身訂做的治療方案。 除監控治療反應,治療準則也建議利用病毒量檢測判定CD4+細胞量> 500 cells/mm3 (病毒量> 100,000 copies/mL)的患者是否應開始進行ART,以及確保抗藥性定序可在適當的患者(患者病毒量> 1,000 copies/mL或ART次優病毒量反應)身上成功。產前準備時應進行病毒量檢測,以確定是否須剖腹生產以避免母子垂直感染HIV (懷孕婦女病毒量> 1,000 copies/mL者)。 Cobas HIV-1是以cobas 6800系統和cobas 8800系統進行之病毒量檢驗,cobas HIV-1可檢驗感染者EDTA血漿中HIV-1 RNA的數量,檢驗中使用兩種探針進行檢驗和定量,但檢驗不分辨HIV-1 M群亞型(group M subtypes of HIV-1)與HIV-1 O群和N群(HIV-1 group O and group N);病毒量由對照非HIV-1 RNA披甲定量標準(non-HIV-1 armored RNA quantitation standard,RNA-QS)得出,進行檢體處理時將納入各標本中,RNA-QS的作用是做為監控檢體準備整體過程和PCR放大過程的內部對照組,此外,檢驗中使用三種對照組:強陽性力價(high titer positive) 、弱陽性力價(low titer positive)和陰性對照組(negative control)。 |
|
健保代碼 |
14074C |
|
幾付點數 |
4000點 |
|
自費收費 |
5000元 |
|
委外代檢事項 |
是否接收代檢■是□否 |